Project Description
您知道血中癌細胞現今可經科技檢驗而無所遁形?您知道癌症在影像學還沒產生變化之前,循環腫瘤細胞已能預知此變化之來臨?精準醫療時代來臨之際,文中為您揭開循環腫瘤細胞的神秘面紗。
◎甚麼是循環腫瘤細胞?
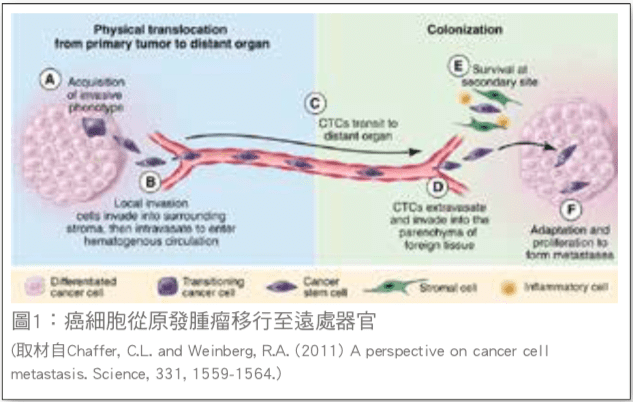
循環腫瘤細胞是一群脫離腫瘤組織進入周邊血液 中的腫瘤細胞【圖 1】,該細胞被認為是導致腫瘤遠端轉移發生的必要前提,其數量可能因為腫瘤本身的 變化或治療的反應而改變,因此偵測其數量可協助評 估癌症預後、治療成效及後續病程發展,臨床醫師藉此擬定更精確的治療方案,又被稱為液態切片 (Liquid biopsy)。是低侵入性採檢,可以替代腫瘤切片作為癌 症預後指標,測定 7.5 毫升血液中循環腫瘤細胞的數量,並於二週給予報告。除了乳癌之外,循環腫瘤細 胞也可臨床應用於轉移性大腸直腸癌、肺癌及攝護腺癌等預後評估。
迄今為止,腫瘤的手術切除以及全身輔助性治療 是早期乳癌的標準治療。儘管成功的初次治療能成功 降低乳癌相關的死亡率,但是早期乳癌經長期追踪仍約有 30% 會產生轉移。這些腫瘤的復發,通常是由於未被藥物或放射線所根治的微小癌細胞轉移擴散,其中許多發生在輔助治療完後數年。未檢測到的微小轉移可能導致乳癌的初次治療失敗,單個癌細胞可能在疾病過程中早期由原發性腫瘤脫落,在體內分散到全身,並作為未來轉移性生長的前兆。不幸的是,通過標準影像方法無法檢測腫瘤細胞從原發腫瘤擴散到遠處部位;因此,找到可以有效檢測系統性微小轉移的新生物標誌物是很重要的議題。為此檢測骨髓中的播散性腫瘤細胞(Disseminated Tumor Cell,DTC) 和周邊血中的循環腫瘤細胞 (Circulating Tumor Cell, CTC)已成為乳癌轉譯研究的重點。骨髓取樣的缺點是屬於侵入性的手術,也因此醫界的研究著重在周邊 血液中較易於取得的 CTC。CTC 可以被認為是微小轉移的替代標誌物,並且可以提供重要的預後和預測信息。
◎如何檢測循環腫瘤細胞?
近年來,隨著許多技術的發展,利用乳癌患者周 邊血中檢測 CTC 的能力越來越成熟。然而 CTC 在血液 中數量非常少,通常每 106 到 108 個單核細胞中只有 1 個,因此它們的分離方法在技術上是一個很大的挑 戰。簡單來說,CTC 在周邊血中處於休眠狀態,只有 一小部分產生會遠處轉移。CTC 的鑑定和表徵需要高 度敏感和特異性。其判定的方法包括濃縮(分離)和 檢測(鑑定)程序的基本組合。收集後,大量白血球 仍殘留在 CTC 的混和液中,可以通過細胞計數策略或 利用於核酸的技術將它們與正常血液細胞區分開來。 再使用免疫細胞化學和分子測定方式區分是否為循環 腫瘤細胞。通常使用下列檢測方法
1. 利用蛋白質技術的方法
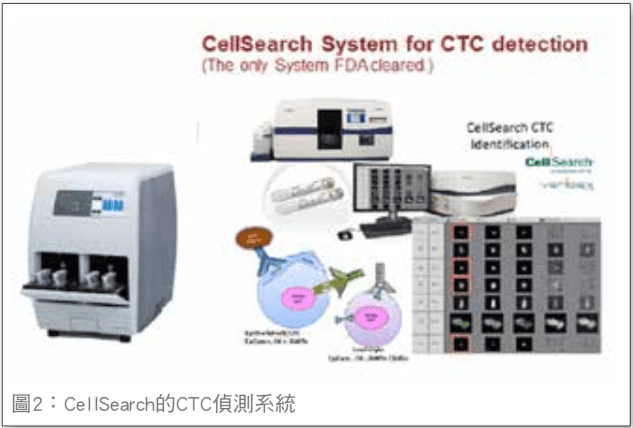
在細胞計數技術中,免疫細胞化學檢測使用單 株抗體,其與在循環的腫瘤細胞上表達但在周圍正 常細胞不表現的標誌物結合。CellSearch 系統它使用 上皮黏附蛋白 (EpCAM) 陽性細胞的半自動收集和通 過 CK8,18 和 19 的免疫螢光染色及 CD45 的陰性來 對 CTC 進行特徵化檢驗。CellSearch 系統和許多其他 CTC 分析使用相同的鑑定方法 ;CK(陽性標記物), CD45(陰性標記物)和核染料(4% 6- 二氨基 -2- 羥 基吲哚,或 DAPI)進行螢光染色。通過螢光顯微鏡 的多色圖像分析,CTC 被定義為 CK+ /CD45- / DAPI + 細胞【圖 2】。
2. 使用核酸技術的方法
利用反轉錄 – 聚合酶鏈反應法 PCR(RT-PCR)測 定活 CTC 所產生的特定 mRNA 的已成為免疫細胞化學 測定的最廣泛使用的替代方法。為了檢測乳腺癌中的 大多數 CTC,多標記方法使用幾種癌症相關基因或上 皮標誌物,CK19 是試驗中最常用的 RNA 標誌物之一 核酸的方法為 CTC 檢測提供了最高的靈敏度。
◎循環腫瘤細胞的臨床應用
CTCs 於轉移性乳癌
轉移性乳癌比早期乳癌更有機會偵測出 CTC, CellSearch 系統敏感度約 10%-25%,陽性發現定義為 7.5-22.5 c.c 血液中有 1 顆以上 CTC,另一反轉錄核酸 技術方法對 CTC 發現敏感度約 41%。利用 CellSearch 系統在轉移性乳癌中發現有 5 顆以上 CTC 的機會約有 50%。但是須注意特異性方面,某些上皮細胞標記可 能暫時表現於正常或未分化的血液、骨髓細胞成份, 例如:MUC1 也會表現於骨髓造血細胞的前驅物。縱 使非常小心的利用檢驗方法分辨出上皮細胞或血液細 胞,但是約 1% 正常人利用 CellSearch 檢驗也會發現 CTC。血液中呈現 CTC 往往意味容易復發、轉移及不 良預後,但也不是化驗出有 CTC 將來就一定會步上復 發、疾病惡化甚至威脅生命結果;學者分析發現血液 中呈現 CTC 者有部分的人在經過 7-15 年追蹤並無疾 病復發。此信息顯示目前檢驗方法偵測出的 CTC,其 中部份細胞在長期後並無使病情惡化的能力。
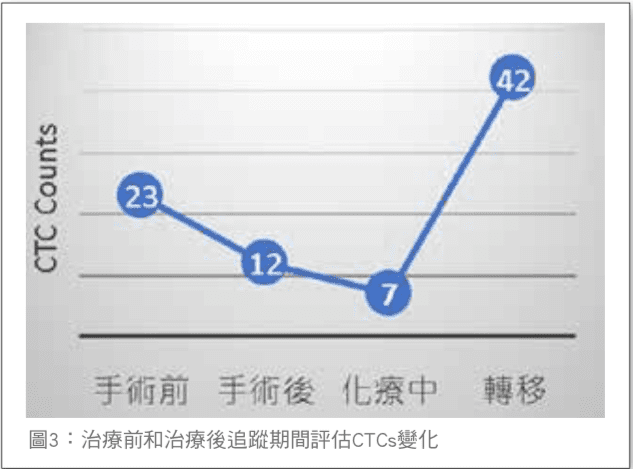
過去為瞭解微小轉移腫瘤細胞常藉由分析骨髓中 散播的腫瘤細胞,然而骨髓的取樣無法如抽血般那 麼方便取樣及可行;現今對於 CTC 的偵測方法 ( 包 括分離、計數及特殊項目查驗 ) 常使用 CellSearch 系 統或 RT-PCR 方法來測驗。CTCs 可以在 40~80% 的 轉移性乳腺癌患者周邊血液中檢測到。大部份有關CTCs 於轉移性乳癌的臨床結果,資料都是來自利用 CellSearch 系統檢驗平台,臨床試驗中證實每 7.5 毫 升血液中若測得 5 顆以上的 CTCs,則在轉移性乳癌 中具有較差的預後。CellSearch 系檢驗平台後續對 乳癌患者系列的研究也使得美國藥物食品管理局在 2004 年批准以 CellSearch 檢驗平台作為評估轉移性 乳癌的預後及監測治療效果。雖然上述結果非常引人 注目,但是確無充分證據告知我們對上述血中不同 CTC 數目者該如何修正治療方法。後來 Liu,海斯等 人對兩大轉移性乳癌病人試驗,同樣證實了在治療前 和治療後追蹤期間評估的 CTCs 的確可有效預測病患預後【圖 3】。
過去為瞭解微小轉移腫瘤細胞常藉由分析骨髓中 散播的腫瘤細胞,然而骨髓的取樣無法如抽血般那 麼方便取樣及可行;現今對於 CTC 的偵測方法 ( 包 括分離、計數及特殊項目查驗 ) 常使用 CellSearch 系 統或 RT-PCR 方法來測驗。CTCs 可以在 40~80% 的 轉移性乳腺癌患者周邊血液中檢測到。大部份有關CTCs 於轉移性乳癌的臨床結果,資料都是來自利用 CellSearch 系統檢驗平台,臨床試驗中證實每 7.5 毫 升血液中若測得 5 顆以上的 CTCs,則在轉移性乳癌 中具有較差的預後。CellSearch 系檢驗平台後續對 乳癌患者系列的研究也使得美國藥物食品管理局在 2004 年批准以 CellSearch 檢驗平台作為評估轉移性 乳癌的預後及監測治療效果。雖然上述結果非常引人 注目,但是確無充分證據告知我們對上述血中不同 CTC 數目者該如何修正治療方法。後來 Liu,海斯等 人對兩大轉移性乳癌病人試驗,同樣證實了在治療前 和治療後追蹤期間評估的 CTCs 的確可有效預測病患預後【圖 3】。
CTCs 對於 HER2 亞型或三陰性乳癌依 然有其預測準確性。此外血中 CTC 上升者較會有機 會在短期內疾病惡化,對於影像上無法或難以偵測評 估的轉移病灶,可利用血中 CTC 作為客觀評量方法。 CTC 數量變化與正子電腦影像顯示病情變化結果吻合 度約 78%,結合正子電腦影像及 CTC 計量數可視為 非常具潛在能力於評估治療反應,尤其適用於一般傳 統影像學對病情難以評估的狀況。與其需執行系列 X 光、骨骼掃描不如妥善應用病情、病史、理學檢查、 肝機能測試、CEA、CA153 及 CTC 數目變化作為病 情變化評量方法。如果後項無輻射檢測方法結果皆正 常那麼在短期幾個月內會從影像上發現病情惡化的機 會不高,那就可免除不方便又造價高昂的影像檢查。 有大於 50% 的病人縱使已發生轉移但卻無法對轉移 病灶作客觀影像評量。截至目前 ASCO 對轉移性乳癌 治療準則尚未將 CTC 計量作為臨床應用準則,然而 從 CTC 所累積的臨床研究資料支持我們應用 CTC 計數檢驗值來互補腫瘤標記 CEA、CA153 在給予特定 治療時參考值,同時提供協助是否需改變治療劑量抑或終止治療甚至應該重新進行影像評估以瞭解病情進 展或惡化。
CTCs 於早期乳癌
手術和輔助治療後,腫瘤細胞的微小轉移擴散可 能持續進展,治療後持續對 CTCs 進行監測可以評估個 體的治療功效,以及識別可能受益於其他治療和 / 或 需要更密切監視的患者。研究報告指出在患有早期乳 腺癌的患者中約 20%至 30%的可於周邊血液中檢測 到 CTCs。
2012 年進行的一項對大約 3000 名早期乳腺癌 患者 CTCs 預後價值的分析顯示,CTCs 的存在與較短 的生存率顯著相關。近期來大型對 I~III 期乳腺癌患 者的研究,其中 20% 的患者被檢測到 CTCs,與未偵 測到 CTCs 的患者相比,其呈現腫瘤較大,具較高的 組織學分級且有較多的淋巴結受到侵犯。CTC 的存在 是無疾病存活期和總存活期的獨立預後因素。在德國 SUCCESS 臨床試驗中,證明 CTCs 可以作為輔助化療 前後存活率的預後評估標誌。其他研究也報導了早期 乳腺癌患者 CTCs 檢測與生存率之間的關聯性。
EpCAM 方法或 RT-PCR 方法可對早期乳癌提供臨 床預後資訊。於 2006 年就有文獻發表利用 RT-PCR 化 驗 167 位無淋巴轉移的早期乳癌病人,經過化學、賀 爾蒙治療併予臨床追蹤結果顯示具 CK-19 mRNA 陽性 患者有較高的復發率及較差的存活率。此外很多研究 發現 CellSearch 系統檢驗法對於 I-III 期乳癌患者若是 7.5cc 血中含有 1 顆或 1 顆以上 CTC 者就容易早期復 發及較差的總存活率。不管用何種檢驗方法,有多篇 研究發現血中持續存在有 CTC 者預後較差。至於在術 前輔助性族群裡,治療反應達到病理完全緩解 (pCR) 與較佳的長期臨床結果相關。術前輔助性化療後 CTCs 的存在可能是治療反應和生存率的替代指標。
綜合結果指出對於早期乳癌,CTCs 能提供預後資訊具臨床確效性 (Clinical Validity),但是如何作為有 效的臨床應用 (Clinical Utility) 目前並不清楚。截至目 前為止,對於早期乳癌 ( 非轉移性乳癌 ) 不管美國臨床 腫瘤醫學會 (ASCO) 或美國國家癌症中心網站 (NCCN) 治療準則,並不建議利用計數循環腫瘤細胞來作為疾 病期數判別或輔助改變治療決策。
◎ CTCs 在轉移性乳癌中扮演 ” 液態切片 ” 的角色
腫瘤細胞特徵表現可能在原發性進展到復發性乳 癌的過程中發生變化。已經有報告顯示腫瘤細胞的基 因型及表現型在原發、次發及轉移位置的型態皆有可 能不同。轉移的腫瘤細胞可能隨時間的變化改變基因 特徵,特別是 CTCs 及轉移腫瘤細胞的雌激素受體 (ER) 和 HER-2 的表現與原發腫瘤不一致。這些不一致性應 該要在轉移處的腫瘤組織被確定,以作為復發、轉移 後的用藥選擇,但是轉移處進行組織切片生檢具有侵 入性且可能存在技術上的困難,例如骨轉移的組織生 檢,而 CTCs 可作為一種低侵入性且即時 ” 液體活組織 檢查 “。
◎結論和未來方向
許多對乳癌患者進行周邊血液中 CTCs 評估的新技 術正在開發中,以便更全面地了解全身性微轉移癌症。 CTCs 已經成為早期和轉移性乳癌中強有力的預後指 標,可能有助於治療策略的優化。此外探討 CTCs 的生 物特性可進一步了解癌症轉移的機制,研究 CTCs 的分 子特徵能進一步得知腫瘤組織的基因組變化,預知可 能的抗藥性以規劃治療方案。如何以 CTCs 檢測輔助治 療規劃,有效避免癌症轉移並降低死亡率仍是臨床上 重要的課題。總體而言,CTCs 是乳癌轉譯研究中一個 令人興奮的領域,可以作為新穎的生物標誌,幫助了 解癌症轉移,預測治療反應及進行新藥開發。
文 / 臺北醫學大學臺北癌症中心副院長暨附設醫院乳房醫學中心主任 杜世興